Поддержите создание крупнейшего раздела на «Онко Вики» — об опухолях головы и шеи
ПоддержатьЛечение рака щитовидной железы радиоактивным йодом
Лечение радиоактивным йодом (131I) — метод системной лучевой терапии, применяется вторым этапом после операции при дифференцированных формах рака щитовидной железы.
Суть радиойодтерапии (РЙТ) в избирательном накоплении 131I остаточными клетками щитовидной железы, включая опухолевые, и их разрушении радиоактивным излучением, при минимальном воздействии на окружающие ткани.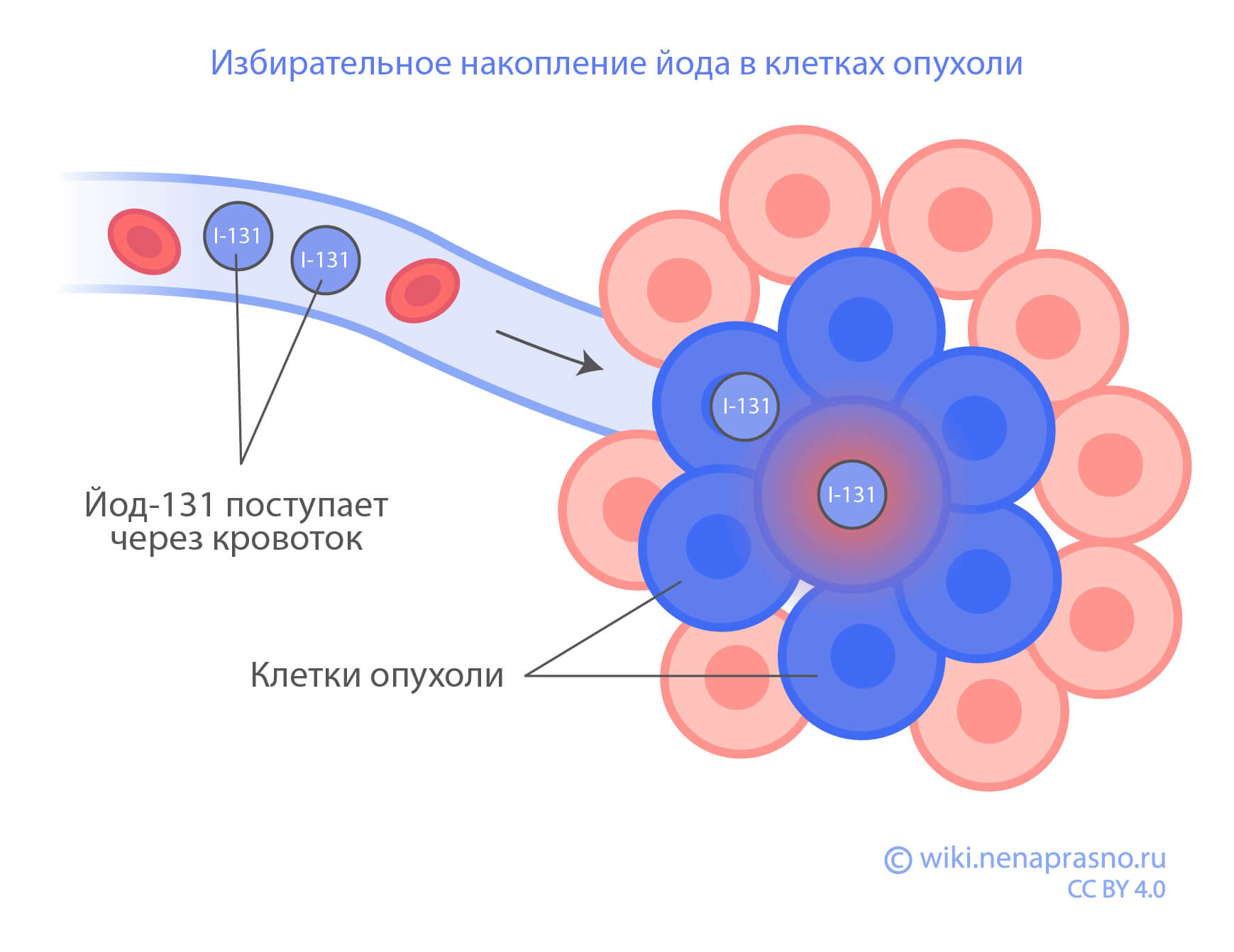
Показания
РЙТ рекомендуется пациентам после полного удаления щитовидной железы:
-
при обнаружении отдаленных метастазов (например, в легкие или кости),
-
структурном рецидиве заболевания, если рак вернулся после первичного лечения,
-
повышенном уровне маркеров опухоли в крови (биохимическом рецидиве), тиреоглобулина (ТГ) и/или антител к тиреоглобулину (АТ к ТГ),
-
опухолях, имеющих высокий и, иногда, промежуточный послеоперационный риск рецидива.
Необходимость радиойодтерапии в зависимости от послеоперационной группы риска рецидива
После удаления щитовидной железы врач получает результаты гистологического исследования (описание клеточного строения опухоли). На основании этого заключения пациента относят к одной из трёх групп послеоперационного риска рецидива, а также принимается первичное решение о необходимости РЙТ.
-
Низкий риск: опухоль ограничена щитовидной железой, отсутствуют признаки агрессивности, нет либо есть единичные микрометастазы в лимфатические узлы шеи.
-
РЙТ не требуется, так как, по данным исследований, не улучшает прогноз.
-
Промежуточный риск: опухоль могла выйти за пределы щитовидной железы, могут быть признаки агрессивности и метастазы в лимфатические узлы шеи.
-
Решение принимается индивидуально, так как нет убедительных данных ни за, ни против. Врач оценивает не только гистологию, но и уровень ТГ и АТ к ТГ, обычно через 3–6 месяцев после операции.
-
Высокий риск: агрессивная опухоль с признаками быстрого роста, крупные (более 3 см) метастазы в лимфатические узлы или их прорастание за пределы капсулы лимфатических узлов, имеются отдаленные метастазы.
-
РЙТ рекомендуется, так как доказано, что она может снизить риск рецидива и улучшить прогноз.
В зависимости от группы риска рецидива также подбирается частота наблюдения и уровень супрессии ТТГ (насколько необходимо снижать уровень ТТГ с помощью заместительной терапии левотироксином натрия).
РЙТ не применяется при медуллярном и анапластическом раке — эти опухоли не накапливают 131I.
Противопоказания
-
Тяжелые сопутствующие состояния в стадии декомпенсации (поражение печени или почек, значимое снижение количества клеток крови, сердечная недостаточность).
Разновидности терапии (дозировки 131I)
-
Лечение метастазов — для уменьшения или уничтожения очагов опухоли (100-200 мКи).
-
Профилактика рецидива (адъювантная терапия) при высоком или промежуточном риске (50-150 мКи).
-
Уничтожение (аблация) остаточной ткани щитовидной железы — для достижения неопределяемого уровня ТГ, АТ к ТГ и упрощения наблюдения (30-50 мКи).
Ограничения до и после лечения
Перед терапией требуется:
-
повышение уровня тиреотропного гормона (ТТГ) гипофиза, что достигается отменой левотироксина за 3–4 недели или инъекциями рекомбинантного человеческого ТТГ (Тироджин, Thyrogen) за 2 дня до РЙТ,
-
исключение йодсодержащих лекарств за 1-2 месяца до РЙТ (контрастные вещества для КТ, антисептические растворы с йодом, амиодарон),
-
низкойодная диета за 7–14 дней до РЙТ (исключаются морепродукты, йодированная соль, йодсодержащие витамины и БАДы; ограничиваются яичные желтки, молочные и некоторые другие продукты),
-
женщинам репродуктивного возраста — тест на беременность (ХГч),
-
кормящим мамам прекращение лактации за 8-12 недель до РЙТ.
После терапии необходимо:
-
избегать близких контактов с людьми (особенно детьми и беременными) в течение нескольких дней после РЙТ, дистанция должна быть не менее 2 метров,
-
избегать беременности не менее 6 месяцев после РЙТ для женщин и зачатия ребенка 2-6 месяцев для мужчин,
-
обеспечить обильное питье (до 2-3 литров жидкости в сутки) и частое мочеиспускание.
Для безопасности родственников и членов семьи в первые дни после РЙТ рекомендовано:
-
не находиться в одной комнате с пациентом,
-
использовать отдельные постель, посуду, санузел,
-
ограничить половые контакты.
Ограничения по близким контактам соблюдают, постепенно смягчая, в течение 1–2 недель после РЙТ, в зависимости от дозировки 131I и остаточного фонового излучения от тела при выписке.
В разных странах действуют разные нормы радиационной безопасности. В России ориентируются на нормативы НРБ‑99/2009, согласно которым безопасным считается уровень излучения менее 20 микрозиверт в час (мкЗв/ч) на расстоянии одного метра. Большинство пациентов достигает этого уровня уже к третьему дню после РЙТ. После этого человек может свободно перемещаться, в том числе путешествовать на самолете или поезде, но рекомендуется иметь при себе справку о прохождении РЙТ, так как остаточное излучение может сохраняться до 3 месяцев и быть зафиксировано рамками или портативными дозиметрами. При этом оно не представляет значимой угрозы для окружающих, если соблюдены основные рекомендации врача.
Порядок проведения РЙТ
Перед лечением учитывается уровень ТТГ и онкомаркеров (ТГ и АТ к ТГ), а также результаты методов визуализации (УЗИ шеи, КТ легких), для оценки распространенности заболевания.
Непосредственно в день РЙТ рекомендуют не есть 2 часа до и после процедуры — так 131I лучше всасывается из кишечника. Пациент выпивает раствор или капсулу с определенной дозой 131I. Процедура безболезненна, по ощущениям не отличается от приема обычной таблетки.
Изоляция в специализированном отделении радионуклидной терапии продолжается 2-3 дня, пока уровень радиации не снизится. На 3-7 сутки сканированием всего тела оценивают распределение 131I в организме. Прием левотироксина возобновляют через 24–48 часов после лечения.
Эффективность
Эффект зависит:
-
от стадии заболевания,
-
возраста пациента,
-
биологических свойств опухоли.
В целом дифференцированный рак щитовидной железы имеет отличный прогноз: 5-летняя общая выживаемость ~ 98,5%. После радикальной операции большинство больных излечивается.
Добавление РЙТ повышает общую выживаемость и снижает частоту рецидивов у пациентов с высоким риском остаточной болезни, например, если опухоль крупных размеров, прорастает в кровеносные сосуды или за пределы щитовидной железы в близлежащие структуры и есть метастазы в лимфатические узлы шеи.
При низком риске рецидивов (например, одиночная микрокарцинома без метастазов) РЙТ не улучшает и без того отличный прогноз. Эффективность РЙТ может снижаться при мутациях в опухоли, таких как BRAF и некоторых других (RET, NTRK), нарушающих захват йода.
К резистентным к радиойодтерапии можно отнести пациентов с изначально не накапливающими 131I метастазами, либо не отвечающих в достаточной степени на РЙТ, с прогрессирующим, несмотря на один или нескольких курсов высокодозной РЙТ, заболеванием.
Когда опухоль прогрессирует и выявлены мутации, к которым есть таргетные препараты (агностический подход), возможно назначение лекарственной терапии с целью редифференцировки опухоли, позволяющей восстановить и/или усилить способность опухолевых клеток к захвату 131I. Это может приводить к более длительной стабилизации заболевания, увеличению выживаемости и снижению потенциального токсического эффекта от длительной таргетной терапии. Подобный подход показывает обнадеживающие результаты и активно используется в специализированных центрах.
Побочные эффекты
Ранние (временные):
-
дискомфорт\болезненность в области шеи,
-
тошнота, реже рвота,
-
изменение вкуса и обоняния,
-
снижение уровня лейкоцитов.
Отсроченные:
-
хроническая сухость во рту из-за воспаления слюнных желез (сиалоаденит),
-
слезотечение из-за повреждения слезных каналов,
-
снижение фертильности (снижение вероятности зачатия ребенка у женщин из-за уменьшения овариального резерва — запаса яйцеклеток в яичниках),
-
крайне низкий риск вторичных опухолей — лейкоза, рака слюнных желез.
Выводы
-
Радиойодтерапия применяется с 1940-х годов при дифференцированном раке щитовидной железы (папиллярном и фолликулярном) в дополнение к хирургическому лечению и основана на накоплении радиоактивного йода опухолевыми клетками и последующем их разрушении.
-
Показания к РЙТ включают высокий и, иногда, промежуточный риск рецидива, наличие отдалённых метастазов, биохимический или структурный рецидив. Не применяется при медуллярном и анапластическом раке, так как клетки этих опухолей не способны захватывать йод.
-
Цель терапии — уничтожение остаточной ткани щитовидной железы и отдаленных метастазов рака щитовидной железы. Выбор дозы зависит от клинической ситуации.
-
Подготовка включает повышение ТТГ (отмена левотироксина или инъекции рекомбинантного ТТГ), исключение йода из лекарств и пищи. Женщинам проводят тест на беременность.
-
Порядок лечения: пациент принимает раствор или капсулу с 131I и изолируется на 2–3 дня в специализированном стационаре. Прием левотироксина возобновляют через 1–2 дня после РЙТ. Перед выпиской проводят диагностическое сканирование и дают дальнейшие рекомендации.
-
После лечения на 1–2 недели ограничивают близкие контакты, особенно с детьми и беременными. Требуется соблюдать меры радиационной безопасности в быту.
-
Эффективность РЙТ зависит от возраста пациента, стадии заболевания и молекулярных особенностей опухоли.
-
Побочные эффекты обычно легкие и кратковременные: боль в шее, тошнота, сухость во рту, изменение вкуса. Реже встречаются хронические осложнения (сиалоаденит, нарушение оттока слезы, снижение фертильности), крайне редко — вторичные опухоли.
-
Большинство пациентов переносят лечение хорошо, осложнения корректируемы, а правильная подготовка и соблюдение рекомендаций повышают безопасность и эффективность РЙТ.
-
При принятии решения о РЙТ должны учитываться все факторы, чтобы избежать необоснованного облучения, но и не упустить возможность улучшения прогноза. Пациенту важно понимать суть процедуры и соблюдать все рекомендации врача до, во время и после лечения.
Что еще почитать?
-
Информация для пациентов про РЙТ при раке щитовидной железы от благотворительной организации исследования рака в Великобритании (на английском языке)
-
Рассказ пациентки о собственном опыте прохождения радиойодтерапии (на русском языке)
- Интервью (видео) о лечении рака щитовидной железы радиоактивным йодом (на русском языке)
Обратитесь к врачу
Наши статьи написаны с учетом принципов доказательной медицины. При подготовке материалов мы обращаемся за консультациями к практикующим врачам и ссылаемся на авторитетные источники. Однако все наши тексты носят рекомендательный характер и не заменяют визит к специалисту.
