Поддержите создание крупнейшего раздела на «Онко Вики» — об опухолях головы и шеи
ПоддержатьХирургия в паллиативных целях при раке пищевода
Цель паллиативной хирургии — снять тяжелые симптомы, вызванные опухолью. Такое лечение не устраняет болезнь, но значительно улучшает качество жизни при неоперабельных и поздних стадиях болезни.
В отличие от некоторых других видов рака, удаление пищевода (эзофагэктомия) в паллиативных целях обычно не выполняется из-за высокого риска осложнений и смертности. Чаще применяются эндоскопические методы контроля симптомов.
Самым частым симптомом при раке пищевода является дисфагия — затруднение при глотании пищи или жидкости. Другой потенциальной проблемой может быть кровотечение из опухоли.
Паллиативные операции при кровотечении
При небольшом продолжающемся кровотечении из опухоли пищевода возможно выполнение эндоскопического гемостаза: через канал эндоскопа проводят специальные инструменты, на конец которых подают энергию, «прижигая» кровоточащие участки.
Паллиативные операции при дисфагии
Пищевод представляет собой полую трубку, по которой проходят пища и вода. Если опухоль деформирует или перекрывает просвет пищевода, возникают трудности при глотании. Чтобы устранить или уменьшить эти ощущения, требуется механическое удаление «лишней» ткани.
Если речь идет о краткосрочной помощи (например, при госпитализации в неспециализированное учреждение), то во время гастроскопии (ЭГДС) с помощью эндоскопа может быть установлен назогастральный зонд. Не рекомендуется использовать его больше 3-4 недель из-за развития нарушений глотания, повышения риска аспирации (попадания пищи в дыхательные пути) и дискомфорта для пациента.
Если устранить дисфагию минимально инвазивными способами, описанными ниже, невозможно, для обеспечения нормального питания может быть предложена установка гастро- или энтеростомы. Стома — это отверстие, созданное хирургическим путем для соединения внутреннего органа с поверхностью тела. Гастростома соединяет переднюю брюшную стенку с желудком, энтеростома — с кишкой. В отверстие устанавливается специальная трубка, по которой в желудочно-кишечный тракт можно вводить пищу и лекарства.

Существует достаточно много вариантов эндоскопических внутрипросветных вмешательств при раке пищевода.
Бужирование
С помощью гастроскопа по струне-проводнику за зону сужения проводят пластиковый зонд (буж), оставляют там на непродолжительное время, затем убирают и меняют на буж большего диаметра. Для получения эффекта необходимо несколько процедур, однако он кратковременный, и уже через 2-4 недели потребуется повторное бужирование. Процедуру проводят вслепую, поэтому выше риски повреждения пищевода. Метод редко применяется в онкологической практике, в основном при доброкачественных болезнях пищевода, сопровождающихся его сужением.
Баллонная дилатация
Через гастроскоп по струне-проводнику проводят специальный прозрачный баллон, который затем «надувают», обеспечивая давление на суженный участок в несколько атмосфер. Прозрачность баллона позволяет визуально контролировать процедуру. Также редко используется в онкологической практике из-за непродолжительного эффекта.
Фотодинамическая терапия
Внутривенно вводят специальный препарат (фотосенсибилизатор), который активно накапливается в тканях опухоли, затем с помощью эндоскопа с лазерным диффузором на опухоль направляют свет определенной волны. Происходит фотохимическая реакция, приводящая к некрозу опухоли. Поскольку препарат накапливается и в здоровых тканях, но с меньшей интенсивностью, он может спровоцировать повышенную чувствительность к солнечным лучам.
Аргоноплазменная коагуляция
Для коагуляции (прижигания) ткани и механического разрушения опухоли используется инертный газ аргон. Эта процедура, как и предыдущие, обладает краткосрочным действием.
Криоабляция
Неконтактный способ, заключающийся в применении экстремального холода (температура при реакции азота до -196о С). Включает в себя фазы заморозки и оттаивания ткани.
Стентирование
Наиболее изученный и широко применяемый в клинической практике метод, обеспечивающий долгосрочный эффект. Установка стента необходима в первую очередь для обеспечения полноценного питания.
Показания к стентированию пищевода:
- наличие неоперабального рака, приводящего к обструкции (непроходимости) пищевода;
- невозможность проведения хирургического или химиолучевого лечения из-за тяжелого состояния пациента;
- местный рецидив заболевания после первичного лечения.
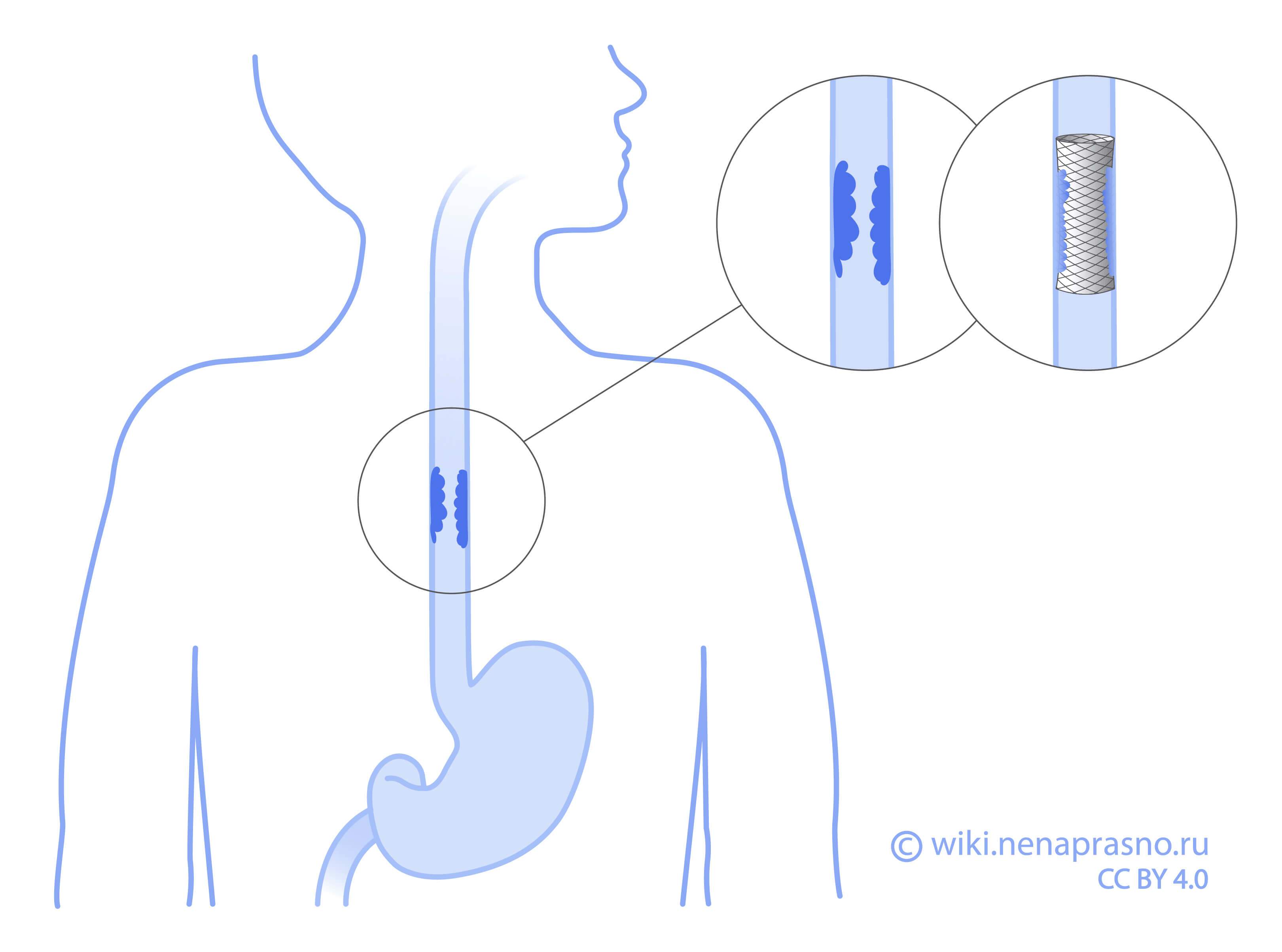
Стентирование пищевода обычно не проводится, если опухоль резектабельна и планируется операция. Однако это не является абсолютным противопоказанием, и оптимальная стратегия лечения пока однозначно не определена. С одной стороны, использование стента перед операцией может ухудшить прогноз и увеличить частоту осложнений. С другой — проведение химиолучевой терапии часто осложняется развитием лучевого эзофагита и усилением дисфагии, а наличие стента в данном случае может обеспечить проходимость пищевода.
Что такое пищеводный стент и как он устанавливается?
Пищеводный стент представляет собой металлическую сетку длинной от 6 до 20 см и диаметром от 10 до 23 мм. Некоторые стенты имеют антирефлюксный клапан, впрочем, его эффективность часто подвергается сомнению.
Стент может быть покрыт специальным веществом полностью или частично, или непокрыт вовсе. Покрытые стенты сдерживают рост опухоли за счет равномерного давления на стенки пищевода и применяются для закрытия свищей. Их можно удалить, но такие стенты чаще непокрытых могут мигрировать ниже и «проваливаться» в желудок. Частично покрытые не имеют покрытия на концах, что позволяет им лучше цепляться за пищевод и обеспечивает меньшую частоту перемещений.
Пищеводные стенты чаще всего сделаны из нитинола — это сплав никеля и титана. С ними безопасно делать МРТ. Однако для полной уверенности в паспорте устройства должна быть указана его безопасность. Силиконовые стенты, как правило, при раке пищевода не применяются.
Стент устанавливают при выполнении ЭГДС под седацией. По специальному проводнику в свернутом виде его доставляет в нужное место, где под контролем камеры эндоскопа расправляют. После процедуры в первые 24-48 часов рекомендован прием только жидкой пищи, затем диета постепенно расширяется. Однако употребление в пищу плотных, крупных продуктов, таких как куски мяса, в дальнейшем не рекомендуется. Если стент установлен в области перехода пищевода в желудок, рекомендуется прием ингибиторов протонной помпы (омепразола, рабепразола) для контроля рефлюкса (заброса желудочного содержимого в пищевод).
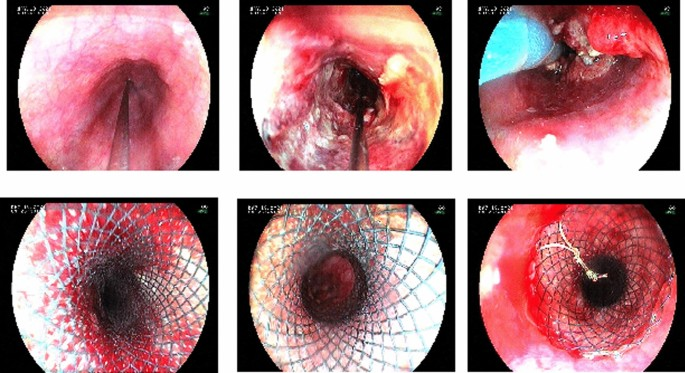
Эффективность стентирования
Для большинства пациентов со злокачественной опухолью пищевода установка стента проходит успешно и значимо снижает симптомы дисфагии. В исследовании 997 пациентов частота успешного стентирования составила 95%, а средняя степень дисфагии уменьшилась с 3 (можно только пить жидкость) до 0 (можно принимать обычную пищу).
Однако несмотря на первоначальный успех, в том же исследовании у 309 пациентов (31%) затрудненное глотание вернулось в среднем через 56 дней. Связано это чаще всего с закупоркой стента растущей опухолью (44%), его перемещением или закупоркой куском пищи (23%).
Как и у любой процедуры, после стентирования могут быть осложнения. К ранним осложнениям относятся:
- боль за грудиной,
- кровотечение,
- повреждение пищевода,
- нарушения дыхания.
Поздние осложнения:
- гастроэзофагеальный рефлюкс,
- прорастание стента,
- миграция стента,
- кровотечение,
- формирование бронхопищеводного или трахеопищеводного свища,
- перфорация пищевода.
Выводы
- Наиболее часто встречающееся осложнение рака пищевода — дисфагия.
- Самым распространенным паллиативным вмешательством по поводу рака пищевода является установка стента.
- Для пациента с опухолью очень важно обеспечить полноценное питание.
Что еще почитать и посмотреть?
- Памятка для пациентов о стентировании пищевода Memorial Sloan Kettering Cancer Center (на русском языке).
- Процедура стентирования пищевода (видео на английском языке).
Обратитесь к врачу
Наши статьи написаны с учетом принципов доказательной медицины. При подготовке материалов мы обращаемся за консультациями к практикующим врачам и ссылаемся на авторитетные источники. Однако все наши тексты носят рекомендательный характер и не заменяют визит к специалисту.