Поддержите создание крупнейшего раздела на «Онко Вики» — об опухолях головы и шеи
ПоддержатьХронический миелоидный лейкоз
Хронический миелоидный лейкоз (ХМЛ) — злокачественное миелопролиферативное заболевание. Приставка «миело-» относится к клеткам костного мозга миелоидной линии дифференцировки, слово «пролиферативный» указывает на активное деление клеток, то есть пролиферацию.
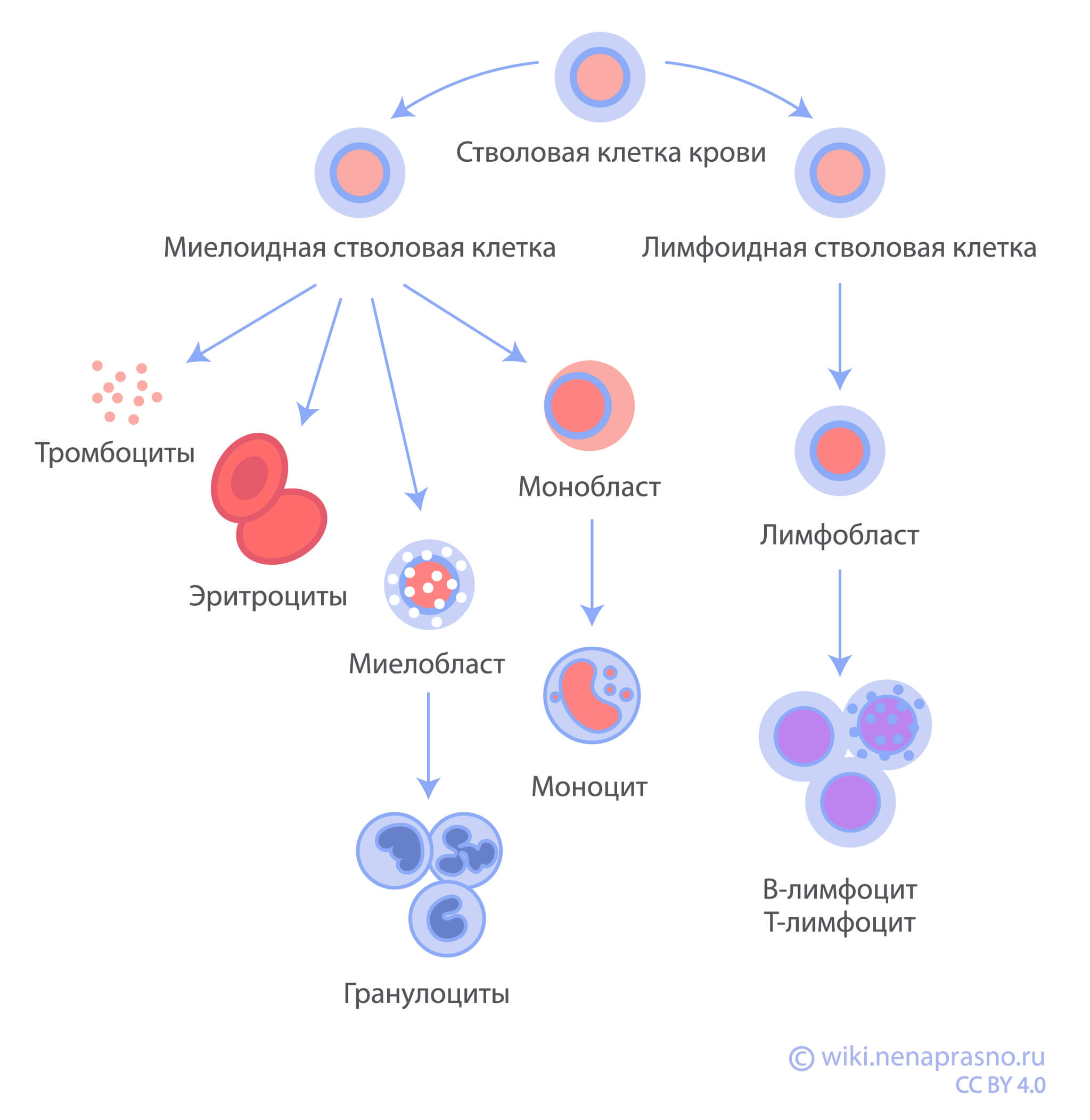
В норме часть стволовых кроветворных клеток становится миелобластами, которые растут, делятся и созревают в лейкоциты, способные бороться с инфекцией. У пациентов с ХМЛ костный мозг начинает вырабатывать аномальные миелобласты, которые неконтролируемо делятся, производя огромное количество клеток – как зрелых лейкоцитов, так и их более ранних форм. Подробнее о видах клеток крови можно почитать здесь.
При ХМЛ в хронической фазе (подробнее о фазах ХМЛ ниже) опухолевый набор клеток обычно представлен зрелыми гранулоцитами и их предшественниками. Эти аномальные клетки не способны противостоять инфекциям, а попадая в кровь в больших количествах, вызывают множество серьезных проблем.
Хронический миелоидный лейкоз (ХМЛ) у детей встречается относительно редко. Он включает примерно 2-3% всех лейкозов у детей в возрасте до 15 лет, и примерно 9% всех лейкемий между 15 и 19 годами.
Причины развития ХМЛ
Неизвестно, что именно вызывает лейкемию – в том числе, ХМЛ. В большинстве детских лейкозов генные мутации и хромосомные аномалии в клетках возникают случайно. Ученые не знают, почему та или иная мутация возникает в клетках человека. Однако почти все случаи ХМЛ связаны с определенным типом генетической аномалии, называемой хромосомной транслокацией.
При этой транслокации часть хромосомы 9 отрывается и присоединяется к части хромосомы 22. Хромосома, возникающая вследствии такой мутации, называется Филадельфийской, так как впервые была открыта в Филадельфии в 1960 году. Это слияние приводит к возникновению нового аномального гена BCR-ABL. Ген BCR-ABL производит фермент тирозинкиназу, который управляет развитием опухолевых клеток, заставляя их бесконтрольно делиться.
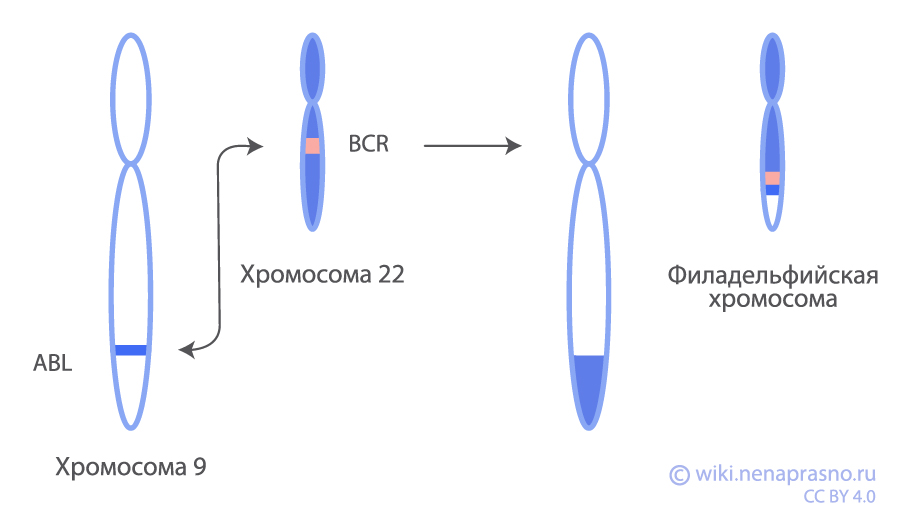
Симптомы ХМЛ у ребенка
В большинстве случаев симптомы зависят от фазы течения заболевания и отличаются у разных пациентов. Выделяют три фазы ХМЛ.
-
Хроническая фаза
Главным критерием этой фазы является наличие менее 10% бластных клеток в крови или костном мозге.
В этот период симптомы лейкемии могут отсутствовать или быть незначительными. Однако в крови и костном мозге выявляются аномальные типы клеток и их ненормально большое количество. Это может быть обнаружено случайно: например, если ребенок сдал общий клинический анализ крови по другой причине. Хроническая фаза может длиться от нескольких месяцев до нескольких лет.
На этом этапе может присутствовать слабость, хуже переносится физическая нагрузка. Периодически могут возникать боли в животе (из-за увеличения печени и/или селезенки), снижение аппетита. Могут наблюдаться повторяющиеся инфекционные заболевания. Сила проявления симптомов индивидуальна.
-
Ускоренная фаза (фаза акселерации)
На этом этапе симптомы вызваны неадекватным образованием патологических клеток в костном мозге и проявляются более интенсивно.
Лабораторно может быть диагностирован эритроцитоз (увеличение количества эритроцитов), тромбоцитоз (увеличение количества тромбоцитов). Им на смену приходит анемия, тромбоцитопения (из-за снижения продукции эритроцитов, тромбоцитов в костном мозге), а также увеличение количества бластов в крови или костном мозге (до 20%). На этом этапе вероятность обнаружения Филадельфийской хромосомы в цитогенетическом анализе составляет 95%.
Клинические проявления могут быть разнообразными. Возможно появление повторяющихся носовых кровотечений, геморрагической сыпи на коже: яркие красные, розовые или бордовые точки на коже и слизистых оболочках, кровоподтеки, не связанные с травмой. Могут развиться серьезные инфекции из-за снижения выработки нормальных лейкоцитов в костном мозге (такие инфекции требуют неоднократного назначения антибактериальной терапии, часто не излечиваются в ожидаемые сроки, требуют госпитализации в стационар).
Могут появиться боли в костях и суставах. Это происходит из-за того, что костный мозг переполнен нормальными и патологическими клетками кроветворения.
Также может наблюдаться увеличение лимфатических узлов (лимфаденопатия). Увеличиваться могут лимфатические узлы любой анатомической группы – в области шеи, подмышечных областей, средостения (что может быть причиной кашля), мезентериальных, забрюшинных (может быть причиной боли в животе) и паховых групп.
-
Бластная фаза (также известная как «бластный криз»)
Основной лабораторный критерий данной фазы заболевания – превышение количества бластов в периферическом анализе крови более 20%.
Это самый опасный период для пациента, требующий немедленной госпитализации для диагностики и лечения. Во время бластной фазы опухолевые клетки активно делятся, но теряют способность дифференцироваться и образовывать зрелые формы (превращаться в гранулоциты и другие клетки). Эту фазу ХМЛ очень трудно отличить от острого лейкоза.
В этой статье перечислены лишь общие, наиболее часто встречаемые симптомы, но они не включают все возможные проявления. Поэтому для постановки точного диагноза необходимо обратиться к специалисту.
Дети и молодые люди, как правило, имеют более агрессивные клинические проявления, чем пожилые люди. Прогностические шкалы для взрослых ХМЛ не применимы к детям.
Диагностика ХМЛ
Помимо полного сбора анамнеза и медицинского осмотра, диагностические процедуры при хроническом миелоидном лейкозе могут включать:
- анализы крови и медицинский осмотр,
- аспирационную и трепан-биопсию костного мозга.
Также проводятся дополнительные лабораторные и визуализационные обследования, необходимые для дифференциальной диагностики ХМЛ (чтобы не принять за него другие заболевания). Чтобы подтвердить диагноз ХМЛ, необходимо выполнить цитогенетическое исследование. У большинства людей с ХМЛ при этом будут обнаружены Филадельфийская (Ph) хромосома и ген слияния BCR-ABL – они и подтвердят диагноз.
Кроме того, цитогенетическое тестирование (FISH, ПЦР) используется для мониторинга эффективности лечения. С помощью этих методов врачи оценивают, сколько опухолевых клеток осталось в организме, и могут сделать выводы об эффективности лечения.
Лечение ХМЛ
Из-за отсутствия надежных клинических данных лечение ХМЛ у детей не имеет единого принятого стандарта. Поэтому педиатры чаще всего следуют рекомендациям, разработанным для взрослых.
В отличие от острых лейкозов, ХМЛ у детей нельзя вылечить никаким типом химиотерапии. Однако в настоящее время широко применяются препараты группы ингибиторов тирозинкиназ (ИТК). Ингибиторы тирозинкиназы представляют собой тип таргетной терапии. То есть эти препараты воздействуют только на определенные типы раковых клеток. При ХМЛ ИТК нацелены на аномальный белок BCR-ABL1, блокируя его функцию. Именно так ИТК вызывают гибель опухолевых клеток.
В настоящее время есть три одобренных ингибитора тирозинкиназы для терапии ХМЛ первой линии в педиатрии – иматиниб, дазатиниб и нилотиниб. Также в настоящее время имеются открытые клинические испытания для применения у детей еще трех препаратов ИТК: бозутиниб, понатиниб, ациминиб.
Как и среди взрослых, более 80% пациентов детского возраста достигают полного цитогенетического (см. ниже) ответа на иматиниб, и более 90% будут живы через 5 лет после постановки диагноза.
Как понять, работают ли ИТК?
Так как ингибиторы тирозинкиназ не излечивает от лейкоза, ответ на лечение ИТК является наиболее важным прогностическим фактором для пациентов с ХМЛ. Он оценивается по трем критериям.
- Гематологический ответ: проводится оценка количества форменных элементов крови – таких как лейкоциты, тромбоциты, незрелые формы гранулоцитов, базофилы. В случае успешного лечения показатели крови постепенно будут стремиться к нормальным значениям. Также признаком гематологического ответа являются нормальные размеры селезенки. Диагностический метод для оценки гематологического ответа – общий анализ крови с лейкоцитарной формулой, полный осмотр пациента, УЗИ органов брюшной полости.
- Цитогенетический ответ: основан на обнаружении клеток костного мозга, имеющих Филадельфийскую хромосому (Ph+). Полный цитогенетический ответ регистрируется при отсутствии Ph-позитивных клеток методом кариотипирования или FISH.
- Молекулярный ответ: исследование, направленное на обнаружение аномального гена BCR-ABL1 в периферической крови или костном мозге методом количественной ПЦР (когда поломку можно не только обнаружить, но и посчитать, в каком количестве клеток она присутствует). Полный молекулярный ответ регистрируется, когда аномальный ген обнаруживается в 0% случаев.
Эти обследования выполняются после постановки диагноза для контроля заболевания и оценки эффективности терапии. Согласно международным рекомендациям, наиболее точным методом для оценки ответа является выполнение количественной ПЦР через определенные промежутки времени (от 3 месяцев до 1 года), то есть производится оценка молекулярного ответа. В ходе лечения можно услышать от врачей термины «длительный глубокий молекулярный ответ» или «длительный полный молекулярный ответ» – это и есть цель лечения ХМЛ.
ТГСК при ХМЛ
Пациенты, которые никогда не достигают молекулярного ответа или теряют его, вероятно, находятся в группе наибольшего риска и являются основными кандидатами для проведения трансплантации гемопоэтических стволовых клеток.
В настоящее время ТГСК является единственным методом полного излечения от ХМЛ у детей. Однако вопрос о необходимости и сроках проведения аллогенной ТГСК в эру ИТК сложен – из-за риска потенциальных осложнений трансплантации. Долгосрочная выживаемость у пациентов с ХМЛ после ТГСК зависит от многих факторов (степени ответа на терапию ИТК, типа трансплантации, общего состояния пациента и др.) и составляет от 66% до 94% по данным разных исследований.
Выводы
- Хронический миелоидный лейкоз характерен для взрослых и крайне редко встречается у детей.
- Ингибиторы тирозинкиназ показывают хорошие результаты в контроле заболевания, однако не способны полностью излечить пациента.
- В настоящее время отсутствуют данные о выраженности побочных эффектов в случае длительного приема ИТК (в течении десятилетий), а значит, неизвестно, насколько их прием безопасен в педиатрической практике.
- Трансплантация гемопоэтических стволовых клеток является единственным методом лечения, позволяющим излечить пациента от ХМЛ.
- Необходимо дальнейшее изучение и клинические испытания течения ХМЛ у детей для лучшего понимания биологии заболевания.
Что еще почитать?
- ХМЛ у детей (сайт St.Jude together, на русском языке).
- Статья и видео о ХМЛ у детей (на английском языке).
Обратитесь к врачу
Наши статьи написаны с учетом принципов доказательной медицины. При подготовке материалов мы обращаемся за консультациями к практикующим врачам и ссылаемся на авторитетные источники. Однако все наши тексты носят рекомендательный характер и не заменяют визит к специалисту.

Материалы подготовлены при поддержке программы “Эффективная филантропия” Благотворительного фонда Владимира Потанина.
