Поддержите создание крупнейшего раздела на «Онко Вики» — об опухолях головы и шеи
ПоддержатьCAR-T и другие виды клеточной терапии при ОЛЛ
Что такое клеточная терапия?
В последнее время в лечении острого лимфобластного лейкоза (ОЛЛ) все более активно применяется клеточная терапия. Это метод лечения онкологических и других заболеваний, основанный на введении пациенту собственных или донорских иммунных клеток крови. К клеточной терапии относятся трансплантация гемопоэтических стволовых клеток (ТГСК), CAR-T-терапия и др.
Преимущество клеточной терапии заключается в том, что она действует избирательно, т.е. направлена только на уничтожение опухоли с наименьшим нанесением вреда здоровым клеткам. В то время как химиотерапия повреждает и другие быстро делящиеся клетки организма, клеточный препарат воздействует только на опухолевые клетки и может быть эффективен при развитии устойчивости опухоли к химиотерапии.
Виды клеточной терапии
- Трансплантация гемопоэтических стволовых клеток (ТГСК). Ее часто относят к клеточной терапии, так как при этом методе собственный процесс кроветворения восстанавливается или же заменяется на донорский. Однако из-за многообразия и сложности метода ТГСК все же выделяется в самостоятельную область изучения.
- После ТГСК возможно дополнительное применение донорских клеток. С помощью специальных технологий из крови или костного мозга донора можно выделить или вырастить в пробирке клетки, способные бороться с вирусными инфекциями или реакцией “трансплантат против хозяина”. Роль введения донорских лимфоцитов (donor leukocyte infusion, DLI) при ОЛЛ в качестве профилактики и лечения рецидива после ТГСК остается спорной — в большинстве исследований эффективность данного вида клеточной терапии крайне низкая.
- Иногда иммунная и клеточная терапия тесно связаны друг с другом. Например, при лечении В-ОЛЛ используется препарат блинатумомаб в сочетании с введением собственных, заранее заготовленных Т-лимфоцитов (так как блинатумомаб сам по себе не уничтожает опухоль, а лишь связывает опухолевую клетку с Т-клеткой организма). С помощью блинатумомаба Т-клетка может “видеть” и уничтожать опухоль. Такой подход необходим, чтобы восполнить потери Т-лимфоцитов, погибших от предшествующего лечения.
- CAR-T-клеточная терапия.
Что такое CAR-T-терапия?
CAR-T-клеточная терапия заключается в извлечении T-лимфоцитов из организма, их модификации и обратном введении пациенту. После модификации Т-лимфоциты способны распознавать, атаковать и разрушать раковые клетки.
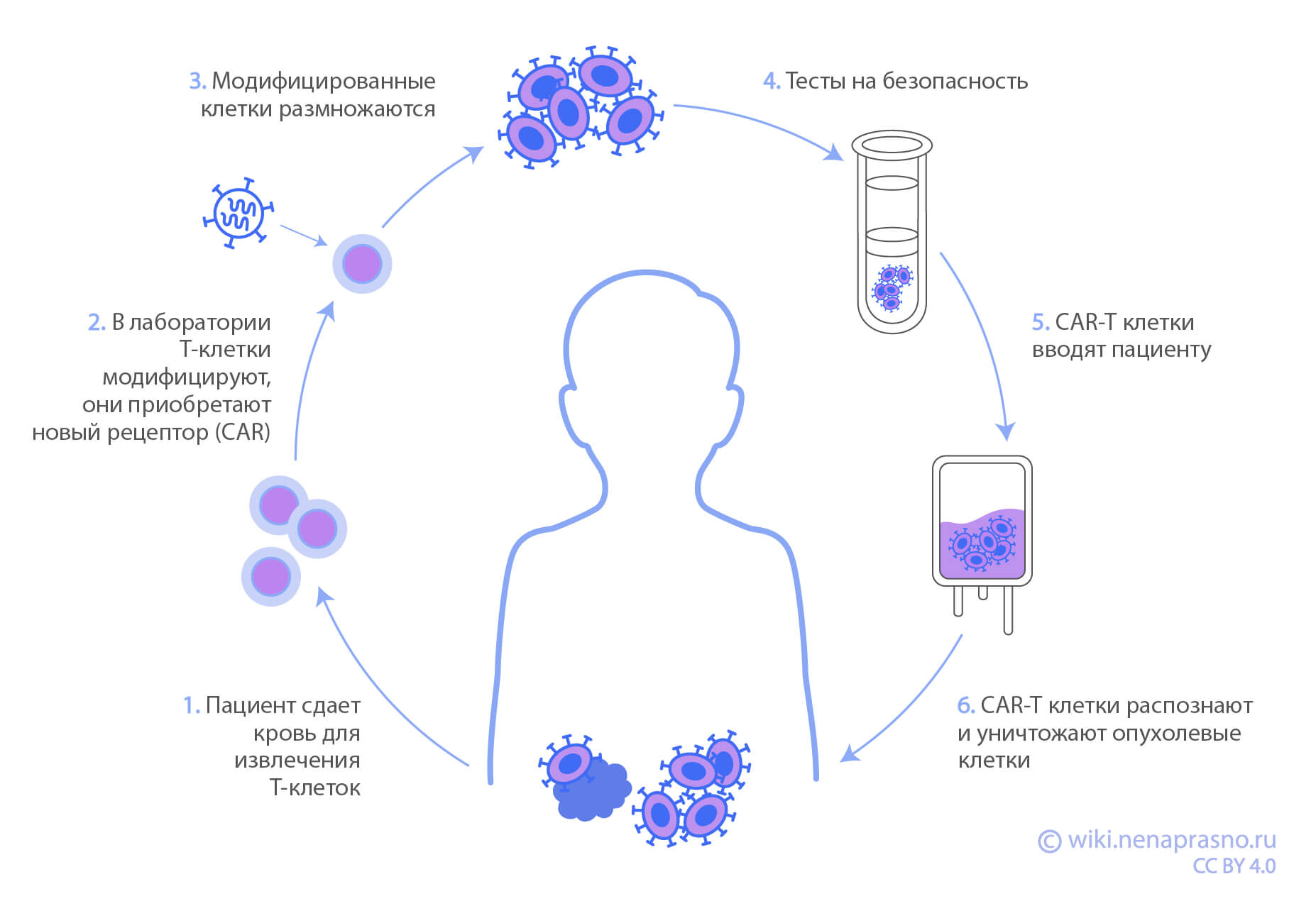
Терапия CAR-T-клетками (Chimeric Antigen Receptor T-Cell, или T-клетки с химерным антигенным рецептором) объединяет три типа современной терапии: клеточную терапию, иммунотерапию и генную терапию. CAR-T-терапия считается клеточной терапией, поскольку пациенту вводится не лекарственное вещество, а собственные или донорские измененные клетки. Также она является иммунотерапией, так как сами клетки иммунной системы пациента борются против раковых клеток. Наконец, это и метод генной терапии, так как проводится генетическая модификация лимфоцитов для борьбы с заболеванием.
Первоначально CAR-T-терапия введена в практику как терапия аутологичными (то есть собственными) клетками пациента. Однако в настоящее время также проводятся исследования терапии аллогенными, то есть донорскими клетками.
Терапия CAR-T-клетками показана пациентам с лейкозом, у которых отмечался по меньшей мере один рецидив после трансплантации костного мозга, или два-три рецидива после применения других методов лечения. В целом, речь идет о пациентах, у которых не удается достичь положительного результата лечения и нет возможности выбрать терапевтический метод среди традиционных средств (химиотерапия, иммунотерапия и трансплантация костного мозга).
В 2017 году препарат тисагенлеклейсел (tisagenlecleucel) стал первым доступным препаратом на основе CAR-T-клеток, одобренным FDA (Food and Drug Administration, Управление по контролю качества пищевых продуктов и лекарственных препаратов США) для лечения детей и молодых людей до 25 лет с В-клеточным ОЛЛ. Препарат зарегистрирован на основании глобального исследования ELIANA, в котором принимало участие 25 исследовательских центров по всему миру. На данный момент зарегистрировано всего 5 CAR-T-препаратов для лечения ОЛЛ, лимфом и множественной миеломы.
Исследование CAR-T-препаратов является перспективным и активно развивающимся направлением. На данный момент во всем мире ведется более 1000 клинических испытаний CAR-T-клеток только для лечения ОЛЛ.
Этапы CAR-T-терапии
1. Аферез – процесс сбора и получения определенного типа клеток (в данном случае – лейкоцитов) пациента или донора. Во время процедуры афереза человек подключен к специальному аппарату, который забирает из вены кровь, отбирает лейкоциты, а все остальные клетки возвращает обратно в кровоток. Процедура может занимать несколько часов, после чего собранные клетки направляются в лабораторию.
2. Изготовление CAR-T-клеток. В лабораторных условиях клетки специально «обучают» распознаванию клеток опухоли и их уничтожению. «Обучение» представляет собой генетическое изменение в геноме Т-лимфоцита. В результате изменения на поверхности клетки появляется специальный химерный (т.е. полученный искусственно) рецептор. Такой рецептор способен «видеть» опухолевые клетки и передавать сигнал на их ликвидацию. Модифицированные T-клетки размножаются, после чего могут быть заморожены и отправлены на хранение или же сразу введены пациенту.
3. Подготовка пациента. Пациенту проводится предварительная химиотерапия, чтобы предупредить возможное отторжение новых клеток организмом и способствовать сохранению и размножению CAR-T-клеток.
4. Инфузия. Подготовленные CAR-T-клетки вводятся пациенту внутривенно в стационаре – подобно переливанию крови.
5. Атака опухолевых клеток. После попадания в кровь пациента концентрат CAR-T-клеток атакует опухолевые клетки, потому что теперь он может их распознавать и уничтожать.
6. Мониторинг. У пациентов, получивших такое лечение, возможны побочные эффекты: лихорадка, боль в мышцах или суставах, низкое кровяное давление, головокружение, неврологические нарушения. В большинстве случаев они не являются тяжелыми, но требуют наблюдения, поэтому пациент остается в стационаре.
Результаты CAR-T-клеточной терапии у детей с ОЛЛ
По данным различных источников 7-9 детей из 10, получивших CAR-T-клеточную терапию для лечения рефрактерного ОЛЛ, достигают ремиссии. Долгосрочного сохранения ремиссии удается достичь примерно 5 детям. Вопрос о том, является ли CAR-T-клеточная терапия самостоятельным методом лечения, остается открытым. Высокое количество рецидивов после CAR-T-терапии (в том числе – поздних) является причиной, по которой многие ученые в мире стремятся провести дополнительные вмешательства после успешно проведенной CAR-T-терапии. В России в центре им. Дмитрия Рогачева в настоящее время применяется стратегия применения ТГСК для закрепления достигнутой ремиссии.
Как и любое другое лечение, CAR-T-клеточная терапия не дает 100% гарантии достижения ремиссии и долгосрочного ее сохранения. Однако комбинация различных методов может существенно повысить шансы пациента на излечение.
Побочные эффекты
Несмотря на ее перспективность, терапия модифицированными Т‑клетками может осложняться некоторыми проблемами, включая токсичность, частичную эффективность и ограниченность применения.
Наиболее опасными осложнениями терапии являются синдром выброса цитокинов (СВЦ) и нейротоксичность. Атакуя опухолевые клетки, CAR-T-лимфоциты воздействуют и на другие клетки иммунной системы, заставляя их массово выделять биологически активные вещества – цитокины. Проявление этого синдрома включает в себя лихорадку, повышение концентрации цитокинов (IL‑6, IFN-γ), пониженное артериальное давление, гипоксию.
Вторым специфическим осложнением терапии является нейротоксичность, или ICANS синдром. Самыми тяжелыми его проявлениями являются судороги и отек головного мозга.
Риск развития тяжелых форм СВЦ и нейротоксичности повышается при большой массе опухоли на момент введения CAR-T-лимфоцитов и высокой дозе вводимых клеток. Токсичность развивается в первые 28 дней от введения клеток и в некоторых случаях может привести к смерти пациента. Ученые продолжают поиск причин, объясняющих развитие тяжелой токсичности, и способов ее избежать.
Ограничения для применения
Одно из препятствий на пути развития терапии CAR-T в России – высокая стоимость реагентов и оборудования для академического производства CAR-T-лимфоцитов, сложность технологии, а также недостаточность правового регулирования. В России ни один коммерческий препарат для терапии CAR-T пока не зарегистрирован, аналоги зарубежных препаратов не производятся. Поэтому разработка и применение CAR-T-клеток в России возможны только в рамках клинических исследований в академических центрах (НМИЦ ДГОИ им. Дмитрия Рогачева, НМИЦ гематологии, НМИЦ онкологии им. Н.Н. Петрова), ведущих свои исследования в области данной технологии.
Подводя итог, можно сказать, что технология CAR-T-клеточной терапии позволяет достичь ремиссии у пациентов с трудноизлечимыми формами ОЛЛ. В ряде случаев это возможно без использования агрессивной химиотерапии или иммунотерапии. В перспективе эта технология может заменить некоторые этапы интенсивной химиотерапии и обеспечить выздоровление пациентов без тяжелых побочных эффектов.
Выводы
- Клеточная терапия – это метод лечения с помощью иммунных клеток донора или самого пациента.
- Терапия CAR-T-клетками–- инновационный и высокоэффективный метод борьбы с ОЛЛ. Он заключается в введении пациенту собственных видоизмененных лимфоцитов, которые могут атаковать опухолевые клетки.
- Ограничениями технологии являются: специфическая токсичность, высокое количество рецидивов без применения последующего лечения, очень высокая стоимость, сложность технологии производства и правового регулирования в РФ.
- CAR-T-клеточная терапия дает надежду пациентам с ОЛЛ, перенесшим уже не один безрезультатный этап лечения. Однако эта технология всё ещё нуждается в совершенствовании для широкого применения.
Что еще почитать и посмотреть?
- Терапия CAR-T-клетками: руководство для пациентов и лиц, ухаживающих за больными (Memorial Sloan Kettering Cancer Center) (на русском языке).
- Видео о CAR-T-клеточной терапии от Beckman Coulter (на английском языке).
Обратитесь к врачу
Наши статьи написаны с учетом принципов доказательной медицины. При подготовке материалов мы обращаемся за консультациями к практикующим врачам и ссылаемся на авторитетные источники. Однако все наши тексты носят рекомендательный характер и не заменяют визит к специалисту.

Материалы подготовлены при поддержке программы “Эффективная филантропия” Благотворительного фонда Владимира Потанина.
