Поддержите создание крупнейшего раздела на «Онко Вики» — об опухолях головы и шеи
ПоддержатьТрансплантация гемопоэтических стволовых клеток при ОМЛ
Роль аллогенной ТГСК в лечении пациентов с ОМЛ
За последние три десятилетия результаты лечения детей с острым миелоидным лейкозом (ОМЛ) значительно улучшились: выздоравливают 70-75%. Во многом это улучшение связано с развитием сопроводительной терапии и применением интенсивных методов лечения, включая проведение трансплантации гемопоэтических стволовых клеток (ТГСК).
Решение о проведении трансплантации должно быть индивидуальным. При его принятии учитываются возраст ребенка, текущее клиническое состояние, наличие альтернативных вариантов лечения, риски и возможные осложнения, связанные с трансплантацией.
Каким пациентам с ОМЛ нужна ТГСК?
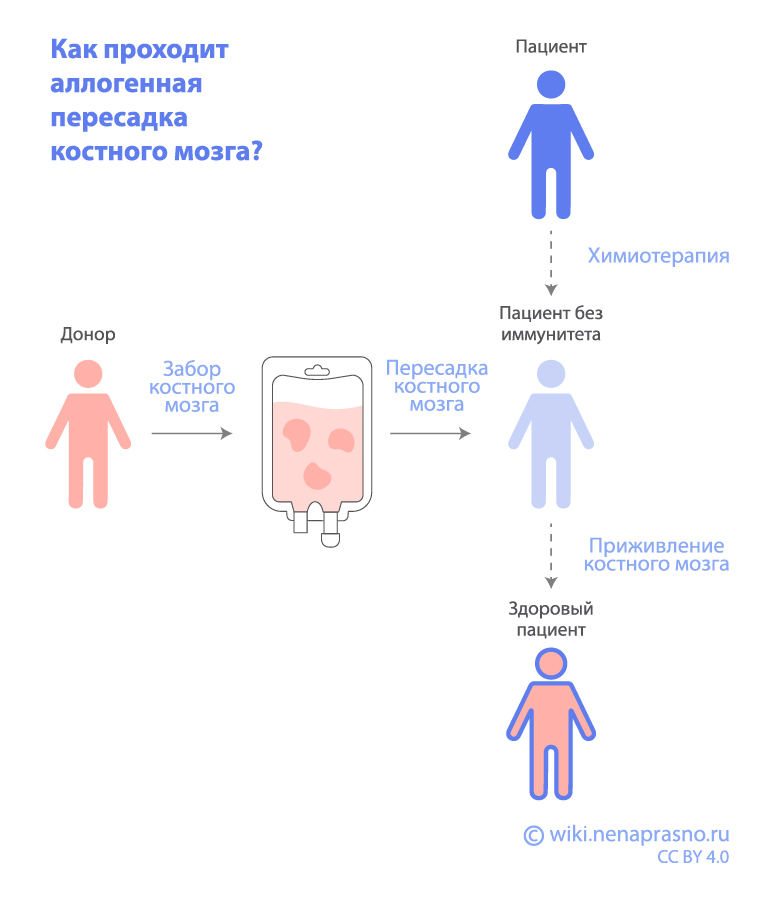
Большинство пациентов с ОМЛ, получающих химиотерапию, достигают полной ремиссии. Однако у части пациентов ремиссия сохраняется непродолжительное время, если не проводить дальнейшее лечение. Для пациентов с высоким риском развития рецидива применяется аллогенная ТГСК – метод, который позволит повысить вероятность выздоровления. При аллогенной трансплантации клетки поступают от донора.
К группе высокого риска относятся пациенты с такими проявлениями заболевания:
- неблагоприятные генетические изменения (мутации) в опухолевых клетках;
- развившийся рецидив заболевания, второй и последующие рецидивы;
- рефрактерное течение (форма заболевания, когда опухоль плохо отвечает на химиотерапию);
- вторичный ОМЛ (развившийся в исходе миелодиспластического синдрома или после другого злокачественного заболевания).
Условия для успешного проведения ТГСК
Статус ремиссии
Для повышения вероятности излечения важно, чтобы на момент ТГСК пациент находился в ремиссии.
Статус пациента
Перед проведением трансплантации обязательно проводится оценка состояния здоровья, функционирования органов и систем пациента. У тех детей, которые на момент трансплантации не имели активных инфекционных заболеваний и осложнений после проведенной химиотерапии, были активны и хорошо питались (в онкологии применяют оценку состояния по шкале Карновского), результаты лечения были лучше.
Выбор донора
Тип донора, а также совместимость донора и реципиента по системе HLA – важные факторы, которые могут повлиять на исход ТГСК. Полностью совместимый сиблинг – брат или сестра – являются самыми лучшими донорами для пациента. Другими подходящими вариантами доноров для трансплантации являются полностью совместимый неродственный донор, гаплоидентичный донор (чаще всего один из родителей или сиблинг пациента). В меньшей степени подходящим будет донор пуповинной крови.
Режим кондиционирования
Кондиционирование – это обязательный этап перед ТГСК. На этом этапе пациенту проводится курс высокодозной химиотерапии или другой лекарственной терапии, которая уничтожает злокачественные клетки и помогает приживлению донорских клеток.
Для ТГСК при ОМЛ используют миелоаблативное кондиционирование. Это лечение вызывает полную аплазию костного мозга (уничтожает максимум его клеток). Такая подготовка помогает достичь противоопухолевого действия (с помощью действия препаратов на злокачественные клетки) и эффекта “трансплантат против опухоли” (когда клетки донора атакуют опухолевые клетки пациента).
Чаще всего для кондиционирования используются такие препараты как треосульфан, флударабин, циклофосфамид, вепезид, мелфалан, бусульфан, тиофосфамид.
Профилактика РТПХ
Реакция “трансплантат против хозяина” (РТПХ) развивается после аллогенной ТГСК, когда клетки донора атакуют “инородные” для них клетки пациента, вызывая иммунный конфликт в организме пациента.
Для того, чтобы предотвратить возникновение РТПХ, используют иммуносупрессивные препараты (препараты, которые подавляют иммунные процессы в организме).
На выбор схемы профилактики РТПХ влияют такие факторы:
- выбор донора (родственный или неродственный),
- степень совместимости донора и реципиента (по системе HLA),
- источник стволовых клеток (костный мозг или периферические стволовые клетки),
- использование технологии удаления Т-лимфоцитов из трансплантата.
Чаще всего для профилактики РТПХ используют такие препараты как циклоспорин и такролимус. Они снижают активацию Т-лимфоцитов (клетки, которые отвечают за возникновение РТПХ). Также могут использоваться циклофосфан, метотрексат, микофенолата мофетил и другие.
Осложнения после ТГСК
Дети, перенесшие ТГСК, имеют риск развития осложнений, связанных с трансплантацией. Есть также риски развития поздних последствий трансплантации (инфекционных и РТПХ) и рецидива заболевания. Вероятность возникновения неблагоприятных эффектов зависит от общего состояния здоровья пациента и статуса заболевания на момент трансплантации, а также от типа ТГСК и возраста пациента. Подробнее о возможных осложнениях читайте здесь.
Прогноз после ТГСК
Важно! Информация о прогнозе может быть чувствительной. Следует знать, что она основана на статистических данных о продолжительности жизни после лечения пациентов с определенным видом рака и не может расцениваться как индивидуальный прогноз. Предсказать, как будет развиваться болезнь, какой будет реакция на лечение, произойдет ли рецидив, и если да, то как скоро — невозможно. Бывает так, что даже при неблагоприятном прогнозе ситуация меняется к лучшему, вопреки статистике. Подробнее об этом читайте в статье «Плохие прогнозы не всегда сбываются»: колонка онколога о статистике и надежде».
Аллогенная ТГСК для детей с рефрактерным ОМЛ или рецидивом заболевания после полной ремиссии успешна в 50% случаев. Результаты ТГСК хуже у детей, которые не достигли ремиссии на момент трансплантации.
Пятилетняя выживаемость у пациентов, получивших трансплантацию во время второй ремиссии, составляет 47%. Результаты ТГСК хуже у пациентов с рецидивом заболевания, не достигших второй ремиссии, а также у пациентов с рефрактерной формой болезни. Пятилетняя выживаемость у таких детей составляет 28% и 17% соответственно.
В случае рецидива заболевания после трансплантации шансы на выздоровление существенно снижаются. Выбор дальнейшего лечения осуществляется на основании возможности достижения повторной ремиссии с помощью химиотерапии, таргетной или клеточной терапии, состоянии пациента (развились ли серьезные осложнения при первой ТГСК), а также возможности быстрого поиска другого донора.
Выводы
- Для пациентов с ОМЛ группы высокого риска, а также пациентов с рецидивом или рефрактерным лейкозом ТГСК является единственным методом, который позволяет достичь длительной ремиссии.
- Для того, чтобы добиться максимальной эффективности и снизить риски осложнений ТГСК, важна заблаговременная подготовка пациента к трансплантации.
- Должен применяться индивидуальный подход к каждому пациенту при определении показаний к проведению трансплантации, выбору донора и режиму кондиционирования.
- ТГСК может сопровождаться осложнениями во время и после лечения.
Что еще почитать?
- Клинические рекомендации по лечению ОМЛ (на русском языке).
- Статья о ТГСК при ОМЛ American Cancer Society (на английском языке).
Обратитесь к врачу
Наши статьи написаны с учетом принципов доказательной медицины. При подготовке материалов мы обращаемся за консультациями к практикующим врачам и ссылаемся на авторитетные источники. Однако все наши тексты носят рекомендательный характер и не заменяют визит к специалисту.

Материалы подготовлены при поддержке программы “Эффективная филантропия” Благотворительного фонда Владимира Потанина.
