Поддержите создание крупнейшего раздела на «Онко Вики» — об опухолях головы и шеи
ПоддержатьЧто такое острый лимфобластный лейкоз?
Острые лейкозы (ОЛ) — самые частые онкологические заболевания детского возраста. Это большая группа болезней, часто называемых «рак крови», при которых нарушается работа костного мозга.
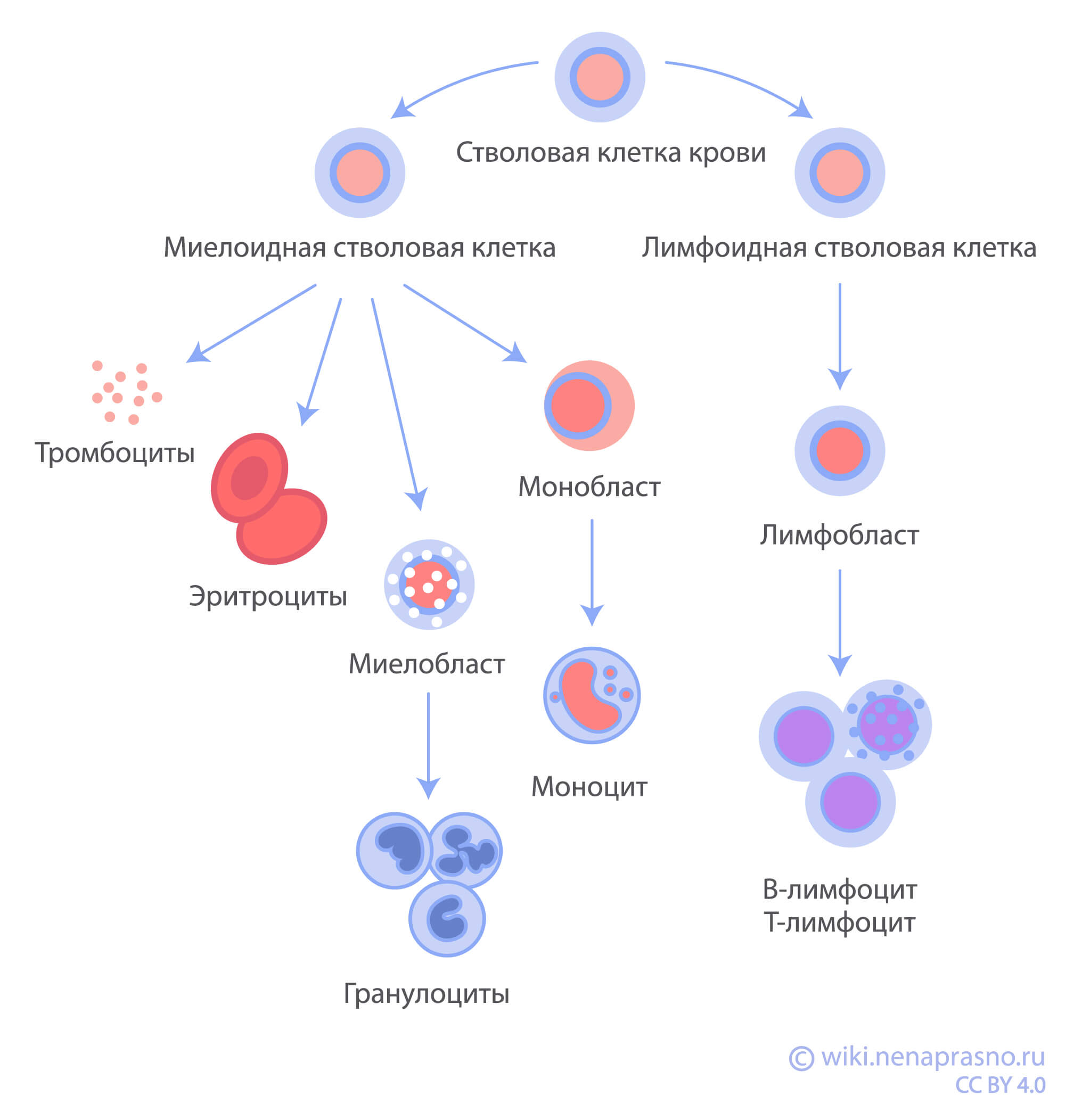
ОЛ возникают из кроветворных (гемопоэтических) клеток костного мозга. При этом опухолевые клетки (бласты) могут развиться из лимфоидных или миелоидных клеток-предшественниц. В зависимости от типа пораженных клеток выделяют острый лимфобластный лейкоз (ОЛЛ) и острый миелобластный лейкоз (ОМЛ).
На долю ОЛЛ приходится до 80% всех лейкозов и около трети всех онкологических заболеваний у детей. Чаще всего ОЛЛ встречается у детей в возрасте от 2 до 5 лет. Это заболевание с одним из самых благоприятных прогнозов: 5-летняя общая выживаемость составляет около 90% в зависимости от группы риска (подробнее о группах риска ниже).
Острый лимфобластный лейкоз возникает при поражении лимфоидной клетки-предшественницы. В норме из такой клетки развиваются лимфоциты — тип лейкоцитов, защищающих организм от разных инфекций. При ОЛЛ возникает «блок дифференцировки» — состояние, при котором молодые и незрелые формы лимфоцитов (лимфобласты) «застревают» на определенном уровне развития и не могут превратиться в зрелые рабочие лимфоциты. Лимфобласты не способны выполнять свою функцию и полноценно защищать организм от инфекций. Кроме того, они очень быстро делятся и заполняют все пространство костного мозга, вытесняя оттуда нормальные кроветворные клетки.

Через некоторое время лимфобласты выходят из костного мозга и с током крови распространяются по всему организму. Все эти процессы вызывают симптомы острого лейкоза.
Классификация и группы риска ОЛЛ
При лейкозе опухолевые клетки находятся в крови и распространяются по всему организму, они могут образовывать скопления в печени, селезенке, лимфатических узлах. Поэтому в отличие от других онкологических заболеваний при лейкозе нельзя установить стадию заболевания.
Вместо стадии определяют группу риска — это вероятность или риск того, что пациента не удастся вылечить или у него будет рецидив болезни. В зависимости от лечебного протокола выделяют разные группы риска: низкий, стандартный (промежуточный), высокий и очень высокий.
При определении группы риска учитывают разные факторы:
- возраст ребенка,
- количество опухолевых клеток в крови,
- тип ОЛЛ,
- наличие особых мутаций в лимфобластах,
- ответ на терапию.
Установление группы риска необходимо, чтобы максимально точно определить прогноз заболевания и выбрать объем лечения для конкретного пациента — достичь эффективности, но не превысить токсичность терапии. Так, пациенты с низкой группой риска получают менее интенсивную терапию и имеют более благоприятный прогноз: 5-летняя бессобытийная выживаемость составляет около 95%. Пациенты из группы очень высокого риска имеют менее благоприятный прогноз — 5-летняя бессобытийная выживаемость составляет до 50%.
Важно! Информация о прогнозе может быть чувствительной. Следует знать, что она основана на статистических данных о продолжительности жизни после лечения пациентов с определенным видом рака и не может расцениваться как индивидуальный прогноз. Предсказать, как будет развиваться болезнь, какой будет реакция на лечение, произойдет ли рецидив, и если да, то как скоро — невозможно. Бывает так, что даже при неблагоприятном прогнозе ситуация меняется к лучшему, вопреки статистике. Подробнее об этом читайте в статье «Плохие прогнозы не всегда сбываются»: колонка онколога о статистике и надежде».
Типы ОЛЛ
В зависимости от типа пораженной клетки-предшественницы ОЛЛ может быть В-клеточным (В-ОЛЛ) или Т-клеточным (Т-ОЛЛ). В-ОЛЛ составляет около 85% от всех ОЛЛ у детей и чаще имеет благоприятный прогноз. T-ОЛЛ составляет 15%, имеет менее благоприятный прогноз и требует более интенсивного лечения.
Существует также дополнительная классификация, которая основана на степени зрелости лимфобластов. У В-ОЛЛ выделяют подтипы: B-I, B-II (самый частый вариант), B-III и B-IV. При B-I ОЛЛ лейкозные клетки представлены совсем молодыми и незрелыми формами, при B-IV ОЛЛ — зрелыми формами. Аналогично классифицируется и Т-клеточный ОЛЛ. Точный тип острого лимфобластного лейкоза определяют методом иммунофенотипирования.
Генетические изменения
Генетические изменения в опухолевых клетках можно обнаружить с помощью цитогенетических и молекулярно-генетических исследований. Они позволяют выявить изменение количества хромосом и найти в ДНК лимфобластов особые генетические перестройки или мутации.
При цитогенетическом исследовании определяется количество хромосом в опухолевой клетке. В норме клетки содержат 46 хромосом — это называется нормальный кариотип. В некоторых опухолевых клетках количество хромосом может быть увеличено — гипердиплоидный кариотип, а в других уменьшено — гиподиплоидный кариотип.
На сегодняшний день выявлено большое количество мутаций, которые могут быть обнаружены в лимфобластах у части пациентов. Некоторые мутации в опухолевых клетках связаны с благоприятным прогнозом, другие свидетельствуют о более тяжелом течении заболевания. Так, например, мутация t(12;21), которая выявляется в 25% случаев В-клеточного ОЛЛ, является благоприятным прогностическим фактором. Другая частая мутация — t(9;22), или «Филадельфийская хромосома», наоборот, является неблагоприятным фактором прогноза. Она требует более интенсивного лечения и добавления в план лечения таргетной терапии.
Ответ на терапию и минимальная остаточная болезнь
Ответ на терапию и уровень минимальной остаточной болезни (МОБ) — очень важные прогностические факторы. В определенные дни лечения, например, на 15-й и 36-й от начала терапии, у пациента берут на исследование образец костного мозга. Оценивают количество опухолевых клеток и МОБ. Выявление большого количества бластов или высокого уровня МОБ свидетельствует об агрессивном течении заболевания и требует перевода пациента в более высокую группу риска.
Другие прогностические факторы
- Возраст ребенка. Прогноз менее благоприятный у детей младше 12 месяцев и старше 10 лет. У пациентов до 1 года ОЛЛ относится к группе инфантильных или младенческих лейкозов. Это заболевание требует интенсивного лечения.
- Количество бластов в крови. Если на момент постановки диагноза в крови выявлено более 50 000 опухолевых клеток, такое состояние называют гиперлейкоцитозом. Данный фактор является неблагоприятным.
- Вовлечение ЦНС или яичек. Если на момент постановки диагноза у ребенка обнаружено поражение центральной нервной системы (ЦНС) или ткани яичек, это также расценивается как неблагоприятный прогностический фактор.
Выводы
- ОЛЛ — самый частый вариант острого лейкоза у детей.
- Чтобы выбрать самый точный план лечения, у пациента с ОЛЛ определяют группу риска.
- Группа риска — вероятность рецидива или отсутствия ответа на лечение у конкретного пациента.
- В зависимости от протокола лечения пациент может быть отнесен к низкой, стандартной (промежуточной), высокой и очень высокой группе риска.
- Основные прогностические факторы, на основании которых определяют группу риска: возраст ребенка, количество лимфобластов в крови, поражение ЦНС и/или ткани яичек, тип ОЛЛ, наличие определенных мутаций в лимфобластах, ответ на терапию и уровень МОБ.
Что еще почитать?
- Раздел про детский ОЛЛ от Cancer Research UK (на английском языке).
- Буклет про детский ОЛЛ от Leukemia and Lymphoma Society (на английском языке).
- Раздел про детский ОЛЛ от Национального института онкологии (на английском языке).
- Справочник по детскому ОЛЛ от NCCN (на русском языке).
- Комикс про ОЛЛ для пациентов и их родителей (на русском языке).
- Психотерапевтическая сказка про лейкоз для детей и их родителей (на русском языке).
Обратитесь к врачу
Наши статьи написаны с учетом принципов доказательной медицины. При подготовке материалов мы обращаемся за консультациями к практикующим врачам и ссылаемся на авторитетные источники. Однако все наши тексты носят рекомендательный характер и не заменяют визит к специалисту.

Материалы подготовлены при поддержке программы “Эффективная филантропия” Благотворительного фонда Владимира Потанина.
